- Differentiële klinische stadiëring van mestceltumoren bij honden met mestceltumoren met een laag en hoog risico
- Inleiding Stadiëring van mestceltumoren
- Belang van prognostische factoren
- Prognostische factoren bij mestceltumoren (MCT's) bij honden
- Belangrijke prognostische factoren
- Gedetailleerde uitleg van de prognostische factoren bij de stadiëring van mestceltumoren
- Diagram van prognostische factoren bij het stadiëren van mestceltumoren
- Tussenconclusie
- Resultaten en discussie van de studie: Differentiële klinische stadiëring van mestceltumoren bij honden met mestceltumoren met een laag en hoog risico
- samenvatting van de resultaten
- bespreking van de resultaten
- conclusie
- Gedetailleerde klinische implicaties van het onderzoek naar mestceltumoren bij honden
- Geïndividualiseerde behandelstrategieën
- Controle en nazorg
- Bijscholing en opleiding van de eigenaren
- conclusie
- Veelgestelde vragen (FAQ's) over mestceltumoren bij honden
- Het belang van het stadiëren van mestceltumoren
- Toepassing van stadiëring van mestceltumoren in therapie
- Prognose gebaseerd op stadiëring van mestceltumoren
- Conclusie
Differentiële klinische stadiëring van mestceltumoren bij honden met mestceltumoren met een laag en hoog risico
Inleiding Stadiëring van mestceltumoren
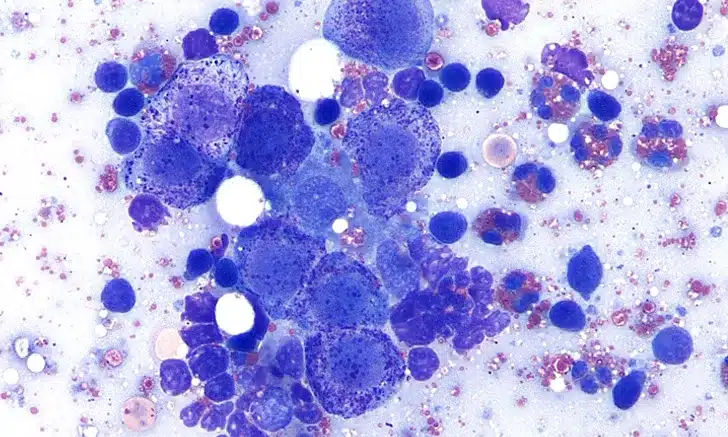
Mestceltumoren (MCT’s) zijn de meest voorkomende kwaadaardige huidtumoren bij honden. Het voorspellen van het gedrag van MCT’s bij honden kan richting geven aan therapeutische aanbevelingen en realistische verwachtingen bieden voor de beheersing of genezing van ziekten op de lange termijn. Verschillende prognostische factoren voor patiënten en tumoren, positief of negatief, worden doorgaans gebruikt om de agressiviteit van MCT's te voorspellen.
De originele studie is hier te vinden: London CA, Thamm DH. Mastceltumoren. In: Withrow SJ, Vail DM, Page RL, red. Withrow en MacEwen's klinische oncologie voor kleine dieren .
5e druk. 2013: 335-380.
Belang van prognostische factoren
Kwalitatieve en kwantitatieve beoordeling van prognostische factoren kan de omvang van therapeutische interventies (bijvoorbeeld chirurgie, bestraling, chemotherapie, remming van receptortyrosinekinase) om de ziekte te beheersen rechtvaardigen. De rol van prognostische factoren bij het begeleiden van de omvang van diagnostische tests voor de klinische stadiëring van MCT's bij honden is echter onvolledig gedefinieerd.
Prognostische factoren bij mestceltumoren (MCT's) bij honden
Mestceltumoren (MCT’s) zijn de meest voorkomende kwaadaardige huidtumoren bij honden. Voorspelling van tumorgedrag speelt een cruciale rol bij het bepalen van de beste therapeutische aanpak en prognose. In dit artikel bespreken we de belangrijkste prognostische factoren die het gedrag en de progressie van MCT’s bij honden beïnvloeden.
Belangrijke prognostische factoren
1. Histologische graad
De histologische graad van een MCT is een van de belangrijkste prognostische factoren. MCT's worden doorgaans geclassificeerd volgens de Patnaik- of Kiupel-systemen:
- Patnaik-systeem:
- Graad I: Goed gedifferentieerde tumoren met een goede prognose.
- Graad II: Matig gedifferentieerde tumoren met variabele prognose.
- Graad III: Slecht gedifferentieerde tumoren met slechte prognose.
- Kiupel-systeem: Maakt onderscheid tussen laaggradige en hoogwaardige tumoren, waarbij hoogwaardige tumoren een slechtere prognose hebben.
2. Grootte en locatie van de tumor
- Grootte: Grotere tumoren hebben doorgaans een slechtere prognose omdat ze vaker metastaseren.
- Locatie: Tumoren op bepaalde locaties, zoals de ledematen, de mond en het perianale gebied, hebben een slechtere prognose.
3. Markers voor celproliferatie
Markers zoals Ki-67-expressie en het mitotische getal geven informatie over de snelheid van celdeling. Een hoge proliferatiesnelheid gaat gepaard met een slechtere prognose.
4. Genetische mutaties
Mutaties in het c-KIT-gen zijn in veel MCT's aanwezig en beïnvloeden de prognose. Tumoren met c-KIT-mutaties reageren vaak op tyrosinekinaseremmers, waardoor de therapeutische opties toenemen.
5. Betrokkenheid van de lymfeklieren
Betrokkenheid van regionale lymfeklieren is een belangrijke negatieve prognostische factor. Metastase naar de lymfeklieren gaat gepaard met een slechtere prognose.
6. Ulceratie en groeisnelheid
- Ulceratie: Tumoren die zweren hebben een slechtere prognose.
- Groeisnelheid: Snelgroeiende tumoren zijn doorgaans agressiever en hebben een slechtere prognose.
7. Herhaling
Herhaling van MCT's na behandeling is een sterk negatief prognostische factor en duidt op agressiever tumorgedrag.
Gedetailleerde uitleg van de prognostische factoren bij de stadiëring van mestceltumoren
Histologische graad
De histologische kwaliteit is gebaseerd op microscopisch onderzoek van tumorweefsel. Graad I-tumoren hebben doorgaans een laag invasief potentieel en een hoog genezingspercentage na volledige chirurgische verwijdering. Graad III-tumoren vertonen daarentegen vaak agressief gedrag met een hoog aantal metastasen en een slechte respons op de behandeling.
Grootte en locatie van de tumor
De grootte van de tumor bij diagnose is een cruciale factor. Tumoren groter dan 3 cm hebben een grotere kans op uitzaaiing. De locatie van de tumor heeft ook invloed op de prognose. Tumoren op minder toegankelijke of gevoelige plaatsen zijn moeilijker volledig te verwijderen en hebben doorgaans een hoger recidiefpercentage.
Markers voor celproliferatie
De expressie van proliferatiemarkers zoals Ki-67 kan worden gemeten door middel van immunohistochemie. Hoge Ki-67-expressie correleert met een hogere celdelingssnelheid en een slechtere prognose. Het mitotische getal, dat wil zeggen het aantal delende cellen in een bepaald gebied, is ook een belangrijke indicator.
Genetische mutaties
Mutaties in het c-KIT-gen leiden tot ongecontroleerde celproliferatie. Deze mutaties kunnen worden gedetecteerd met behulp van PCR en sequencing. De aanwezigheid van c-KIT-mutaties kan de prognose verslechteren, maar biedt ook kansen voor gerichte therapie met tyrosinekinaseremmers zoals toceranib of masitinib.
Betrokkenheid van de lymfeklieren
Fijne naaldaspiratie en cytologisch onderzoek van regionale lymfeklieren zijn belangrijk om de verspreiding van de ziekte te evalueren. Positieve lymfeklieren zijn een teken van systemische verspreiding en een slechtere prognose.
Ulceratie en groeisnelheid
Zwerende tumoren zijn vatbaar voor ontstekingen en infecties, wat de behandeling bemoeilijkt en de prognose verslechtert. De snelheid waarmee een tumor groeit, kan ook een indicator zijn voor de agressiviteit ervan.
Herhaling
Het terugkeren van de tumor na behandeling duidt vaak op onvolledige chirurgische verwijdering of bijzonder agressief tumorgedrag. Vaak is hiervoor een intensievere en uitgebreidere vervolgbehandeling nodig.
Diagram van prognostische factoren bij het stadiëren van mestceltumoren
Tussenconclusie
Een uitgebreide beoordeling van de bovengenoemde prognostische factoren is cruciaal voor het bepalen van de beste therapeutische benaderingen en het voorspellen van de progressie van mestceltumoren bij honden. Zorgvuldige analyse van deze factoren kan de levenskwaliteit en overleving van getroffen honden helpen verbeteren.
Wij hopen dat deze gedetailleerde uitleg van de prognostische factoren bij MCT’s u waardevol inzicht zal verschaffen en zal bijdragen aan een betere zorg voor onze viervoeters.
Resultaten en discussie van de studie: Differentiële klinische stadiëring van mestceltumoren bij honden met mestceltumoren met een laag en hoog risico
De huidige retrospectieve studie analyseerde de prognostische betekenis van diagnostische tests bij honden met mestceltumoren (MCT's). In het bijzonder werd de waarde van uitgebreide klinische stadiëring bij honden met MCT's met hoog en laag risico onderzocht.
samenvatting van de resultaten
Klinische stadiëring van MCT's met een laag risico
Uit de studie bleek dat uitgebreide diagnostische tests geen significante prognostische meerwaarde bieden bij honden met MCT's met een laag risico. Honden met MCT’s met een laag risico die geen negatieve prognostische factoren hadden, zoals hooggradige lymfekliermetastasen of snelle tumorgroei, profiteerden niet van intensieve klinische stadiëring. Deze tests omvatten abdominale echografie, aspiratie van milt en lever, thoracale radiografie en cytologisch onderzoek van regionale lymfeklieren.
Belangrijkste leerpunten:
- Geen verbetering van de prognose: Uitgebreide stadiëring resulteerde niet in betere prognoses of langere overlevingstijden bij honden met MCT's met een laag risico.
- Verminderde behoefte aan invasieve tests: Omdat uitgebreide stadiëring geen extra voordeel opleverde, kunnen invasieve tests worden verminderd bij honden met MCT's met een laag risico, waardoor stress en kosten voor eigenaren worden geminimaliseerd.
Klinische stadiëring van MCT's met een hoog risico
Honden met MCT’s met een hoog risico hebben daarentegen aangetoond dat uitgebreide diagnostische tests een waardevol prognostisch hulpmiddel bieden. MCT's met een hoog risico werden gekenmerkt door de aanwezigheid van negatieve prognostische factoren zoals een hoge histologische graad, lymfekliermetastasen, snelle groei, ulceratie of terugkeer van de tumor.
Belangrijkste leerpunten:
- Verhoogd aantal metastasen: Honden met MCT’s met een hoog risico hadden een grotere kans om metastasen op afstand te ontwikkelen bij de diagnose of tijdens het verloop van de ziekte.
- Kortere overleving: Deze honden hadden kortere overlevingstijden vergeleken met honden met MCT's met een laag risico, wat het belang van intensievere monitoring en behandeling benadrukt.
- Voordelen van uitgebreid testen: Uitgebreide klinische stadiëring maakte een nauwkeurigere beoordeling van de ziekteverspreiding mogelijk en hielp bij het ontwikkelen van op maat gemaakte behandelplannen.
bespreking van de resultaten
Prognostische betekenis van klinische stadiëring
De onderzoeksresultaten benadrukken dat klinische stadiëring cruciaal is bij het beoordelen van de ziekteprognose, maar op verschillende manieren moet worden toegepast, afhankelijk van de risicostatus van de tumor.
MCT's met een laag risico
- Rationalisatie van diagnostische procedures: Voor honden met MCT's met een laag risico is rationeel gebruik van diagnostische tests zinvol om onnodige stress te voorkomen. Een gedetailleerd histologisch onderzoek van de tumor en de beoordeling van minder invasieve tests zijn vaak voldoende om een goede prognose te maken.
MCT's met een hoog risico
- Uitgebreide diagnose vereist: Voor MCT's met een hoog risico is een alomvattende diagnostische aanpak noodzakelijk om de best mogelijke prognose en behandeling te garanderen. Dit omvat het gebruik van geavanceerde beeldvormingstechnieken en cytologische tests om de volledige omvang van de ziekteverspreiding te beoordelen.
Klinische implicaties
De studie biedt waardevolle richtlijnen om de klinische praktijk te verbeteren bij de behandeling van honden met MCT’s:
- Geïndividualiseerde behandelstrategieën: De bevindingen benadrukken de noodzaak van geïndividualiseerde behandelstrategieën gebaseerd op de specifieke prognostische factoren van elke hond.
- Benaderingen die hulpbronnen besparen: Voor MCT's met een laag risico kan het verminderen van uitgebreide diagnostische tests hulpbronnen besparen en tegelijkertijd een hoge kwaliteit van de behandeling garanderen.
- Intensieve monitoring voor MCT's met hoog risico: Voor honden met MCT's met hoog risico is intensieve monitoring en proactieve behandeling essentieel om de best mogelijke kwaliteit van leven en overleving te bereiken.
conclusie
Concluderend laat de studie zien dat gedifferentieerde klinische stadiëring op basis van de specifieke prognostische factoren van MCT's met een laag en hoog risico cruciaal is voor de prognose en behandeling van honden met mestceltumoren. Hoewel een spaarzamer gebruik van diagnostische tests voldoende kan zijn voor MCT's met een laag risico, vereist de behandeling van MCT's met een hoog risico een alomvattende en intensieve diagnostische aanpak.
Wij hopen dat deze gedetailleerde presentatie van de onderzoeksresultaten en discussie u waardevol inzicht zal verschaffen en de behandeling en prognose van onze viervoeters zal helpen optimaliseren.
Gedetailleerde klinische implicaties van het onderzoek naar mestceltumoren bij honden
De bevindingen van deze studie bieden waardevolle richtlijnen voor de klinische praktijk bij de behandeling van honden met mestceltumoren (MCT's). De gedifferentieerde afweging van MCT's met hoog en laag risico maakt een gerichte en zachte behandeling mogelijk die zowel de kwaliteit van leven als de overlevingstijd van de getroffen honden optimaliseert.
Geïndividualiseerde behandelstrategieën
MCT's met een laag risico
Voor honden met MCT’s met een laag risico is het belangrijk om zorgvuldig diagnostische en therapeutische maatregelen te overwegen:
- Minder invasieve diagnostiek: Omdat uitgebreid testen bij deze honden geen significante prognostische waarde oplevert, kunnen minder invasieve procedures zoals eenvoudige chirurgische biopsieën en basisbloedonderzoek voldoende zijn.
- Kosten- en hulpbronnenefficiëntie: Het vermijden van uitgebreide en dure diagnostische procedures beschermt de financiële middelen van de eigenaren en minimaliseert stress voor de dieren.
- Focus op histologisch onderzoek: Nauwkeurige histologische analyse van het tumorweefsel blijft echter cruciaal voor het bepalen van de tumorgraad en het beoordelen van de prognose.
MCT's met een hoog risico
Voor honden met MCT’s met hoog risico zijn uitgebreidere diagnostische en therapeutische benaderingen vereist:
- Geavanceerde beeldvormingstechnieken: Technieken zoals computertomografie (CT) of magnetische resonantie beeldvorming (MRI) kunnen helpen om de verspreiding van de tumor en de aanwezigheid van metastasen nauwkeuriger te bepalen.
- Cytologisch onderzoek: Fijne naaldaspiraties en biopsieën van regionale lymfeklieren en mogelijke metastasen op afstand zijn cruciaal om het volledige klinische beeld vast te leggen.
- Multimodale therapeutische benaderingen: De behandeling moet een combinatie van chirurgie, bestralingstherapie en chemotherapie omvatten om de tumorgroei onder controle te houden en te voorkomen dat deze zich verspreidt.
Controle en nazorg
Regelmatige controles
Ongeacht de risicostatus van de tumor zijn regelmatige controles belangrijk:
- Vroegtijdige detectie van recidieven: Regelmatig onderzoek maakt een vroege detectie en behandeling van tumorrecidieven mogelijk, wat de prognose kan verbeteren.
- Aanpassing van de therapie: Op basis van de controlebevindingen kunnen therapeutische maatregelen worden aangepast om optimaal op het beloop van de ziekte te reageren.
Kwaliteit van leven en palliatieve zorg
Bij de behandeling van honden met MCT’s ligt de focus niet alleen op het verlengen van de overlevingstijd, maar ook op het behouden en verbeteren van de kwaliteit van leven:
- Pijnbestrijding: Effectieve pijntherapie is essentieel om het welzijn van honden te garanderen.
- Voedingsondersteuning: Een aangepast dieet kan het immuunsysteem helpen versterken en de algehele gezondheid verbeteren.
- Palliatieve maatregelen: Als de ziekte gevorderd is, kunnen palliatieve maatregelen zoals pijnstillers en ontstekingsremmende medicijnen worden gebruikt om de symptomen te verlichten en de kwaliteit van leven te behouden.
Bijscholing en opleiding van de eigenaren
Het opleiden en ondersteunen van huisdiereigenaren speelt een belangrijke rol:
- Informatie over prognose en behandelingsopties: Dierenartsen moeten eigenaren volledig informeren over de prognose en verschillende behandelingsopties, zodat ze weloverwogen beslissingen kunnen nemen.
- Emotionele steun: Een diagnose van MCT kan emotioneel stressvol zijn voor eigenaren. Medelevende begeleiding en ondersteuning van het veterinaire team is daarom essentieel.
conclusie
De gedetailleerde beschouwing van de klinische implicaties van het onderzoek naar mestceltumoren bij honden toont het belang aan van een geïndividualiseerde en zorgvuldig op maat gemaakte behandelstrategie. Door rekening te houden met specifieke prognostische factoren en de therapie op maat te maken, kunnen zowel de kwaliteit van leven als de overlevingstijd van getroffen honden worden verbeterd.
Wij hopen dat deze gedetailleerde presentatie van de klinische implicaties u waardevol inzicht zal verschaffen en de behandeling en verzorging van onze viervoeters zal helpen optimaliseren.
Veelgestelde vragen (FAQ's) over mestceltumoren bij honden
Wat zijn mestceltumoren en hoe vaak komen ze voor bij honden?
Mestceltumoren (MCT’s) zijn kwaadaardige huidtumoren die ontstaan uit mestcellen.
Mestcellen zijn een soort witte bloedcellen die een belangrijke rol spelen in het immuunsysteem, vooral bij allergische reacties en de verdediging tegen parasieten. MCT's zijn de meest voorkomende huidtumoren bij honden en kunnen in verschillende vormen en ernst voorkomen. Ze variëren van langzaam groeiende, goed gedifferentieerde tumoren tot agressieve, slecht gedifferentieerde tumoren die snel kunnen uitzaaien. De frequentie van MCT's varieert afhankelijk van het hondenras, de leeftijd en het geslacht. Bepaalde rassen zoals Boxers, Boston Terriers, Labrador Retrievers en Golden Retrievers lopen een groter risico om MCT’s te ontwikkelen. Ook oudere honden zijn gevoeliger voor deze tumoren, hoewel ze ook bij jongere honden kunnen voorkomen.
Welke symptomen kunnen wijzen op een mestceltumor?
Symptomen van mestceltumoren bij honden kunnen sterk variëren, afhankelijk van de locatie en progressie van de tumor.
De meest voorkomende symptomen zijn: Knobbeltjes of zwelling op de huid: deze kunnen klein en onopvallend zijn, of groot en duidelijk zichtbaar.
MCT's voelen vaak stevig aan en kunnen vrij bewegen of stevig aan de onderliggende huid hechten. Huidveranderingen: De huid boven de tumor kan rood, gezwollen of zweren zijn.
Jeuk en irritatie: Omdat mestcellen histamine afgeven, kunnen tumoren jeuk en irritatie veroorzaken.
Braken en diarree: deze symptomen treden op als gevolg van de afgifte van histamine en andere stoffen die de maagwand kunnen irriteren.
Verlies van eetlust en gewichtsverlies: dit zijn veel voorkomende niet-specifieke symptomen bij gevorderde tumoren.
Zwelling en veranderingen in de lymfeklieren: Als de tumor uitzaait, kunnen de regionale lymfeklieren vergroot en pijnlijk zijn.
Als u een verdacht knobbeltje of ongewone zwelling bij uw hond opmerkt, moet u onmiddellijk een dierenarts raadplegen voor een nauwkeurige diagnose.
Hoe wordt een mestceltumor gediagnosticeerd?
Het diagnosticeren van een mestceltumor omvat verschillende stappen:
Klinisch onderzoek: De dierenarts onderzoekt de knobbel en beoordeelt de grootte, vorm, consistentie en positie ervan.
Fijne naaldaspiratie: Met een fijne naald wordt een kleine hoeveelheid cellen uit de tumor verwijderd.
Deze cellen worden vervolgens onder een microscoop onderzocht om te bepalen of het mestcellen zijn. Biopsie: In sommige gevallen is een volledige of gedeeltelijke chirurgische verwijdering van de tumor noodzakelijk om een definitieve diagnose te stellen.
Het verwijderde weefsel wordt histopathologisch onderzocht om de tumorgraad te bepalen. Beeldvormingsprocedures: Als er uitzaaiingen worden vermoed, kunnen beeldvormingsprocedures zoals röntgenfoto's, echografie, computertomografie (CT) of magnetische resonantiebeeldvorming (MRI) worden gebruikt om de verspreiding van de ziekte te beoordelen.
Bloedonderzoek: deze kunnen helpen de algehele gezondheid van de hond te beoordelen en te bepalen of interne organen zijn aangetast.
Een nauwkeurige diagnose is cruciaal om het beste behandelplan voor de hond te ontwikkelen en de prognose in te schatten.
Welke behandelingsmogelijkheden zijn er voor mestceltumoren?
De behandeling van mestceltumoren bij honden hangt af van verschillende factoren, waaronder de graad van de tumor, locatie, grootte en aanwezigheid van metastasen.
Veel voorkomende behandelingsopties zijn: Chirurgie: Volledige chirurgische verwijdering van de tumor is vaak de behandelmethode die de voorkeur verdient.
Het doel is om de tumor te verwijderen met een voldoende veiligheidsmarge om de kans op herhaling te minimaliseren. In sommige gevallen kan een tweede operatie nodig zijn als de tumor niet volledig is verwijderd. Bestralingstherapie: Dit wordt vaak gebruikt na een operatie, vooral als de tumor niet volledig kan worden verwijderd of zich in een gebied bevindt dat moeilijk te opereren is.
Radiotherapie kan ook worden gebruikt voor inoperabele tumoren om hun groei te vertragen en de symptomen te verlichten. Chemotherapie: Chemotherapiemedicijnen worden gebruikt om de resterende kankercellen te doden en het risico op uitzaaiingen te verminderen.
Deze behandeling wordt vaak toegepast bij hooggradige of uitgezaaide tumoren. De combinatie van medicijnen kan worden aangepast om de beste resultaten te bereiken. Tyrosinekinaseremmers: Deze gerichte therapieën, zoals toceranib en masitinib, remmen de groei van kankercellen door specifieke signaalroutes te blokkeren.
Ze zijn vooral effectief bij MCT's met c-KIT-mutaties. Palliatieve behandeling: Bij gevorderde ziekte, wanneer genezing niet langer mogelijk is, richt de behandeling zich op het verlichten van de symptomen en het verbeteren van de levenskwaliteit van de hond.
Dit omvat pijnstillers, ontstekingsremmende medicijnen en ondersteunende zorg. Elke behandeling heeft zijn voor- en nadelen, en de beste aanpak moet worden afgestemd op de hond en zijn specifieke situatie.
Wat is de prognose voor honden met mestceltumoren?
De prognose voor honden met mestceltumoren varieert sterk en is afhankelijk van verschillende factoren:
Histologische graad: De graad van de tumor is een belangrijke prognostische factor.
Laaggradige tumoren (graad I en laaggraad II) hebben meestal een goede prognose en zijn vaak te genezen, vooral als ze volledig worden verwijderd. Hooggradige tumoren (hooggradige II en graad III) hebben een slechtere prognose omdat ze agressiever zijn en vaker metastaseren. Locatie en grootte van de tumor: Tumoren die groeien in moeilijk bereikbare of gevoelige gebieden zoals de mond of het perianale gebied hebben een slechtere prognose.
Grotere tumoren hebben doorgaans ook een slechtere prognose. Aanwezigheid van uitzaaiingen: Honden met uitgezaaide tumoren hebben een slechtere prognose.
Metastasen naar de lymfeklieren, lever, milt of andere organen verslechteren de overlevingskansen aanzienlijk. Celproliferatiemarkers en genetische mutaties: Hoge proliferatiesnelheden en de aanwezigheid van bepaalde genetische mutaties (zoals c-KIT) kunnen de prognose verslechteren.
Deze factoren beïnvloeden de agressiviteit van de tumor en de reactie op de behandeling. Behandelingsaanpak: Vroegtijdige, uitgebreide behandeling, inclusief chirurgie, bestralingstherapie en/of chemotherapie, kan de prognose verbeteren.
Het succes van de behandeling hangt ook af van het vermogen van de dierenarts om de tumor volledig te verwijderen en de therapie op het individu af te stemmen. Over het algemeen hebben honden met laaggradige, gelokaliseerde tumoren een goede prognose met een hoog genezingspercentage na volledige chirurgische verwijdering.
Voor hooggradige of uitgezaaide tumoren kan de prognose slechter zijn, maar met een intensieve en op maat gemaakte behandeling kunnen veel honden nog steeds een bevredigende levenskwaliteit en langdurige overleving bereiken. We hopen dat deze uitgebreide antwoorden u zullen helpen een beter inzicht te krijgen in mestceltumoren bij honden en u zullen helpen beslissen wat de beste handelwijze is voor de gezondheid van uw huisdier.
Samenvatting van de stadiëring van mestceltumoren bij honden
Stadiëring van mestceltumoren (MCT's) bij honden is een cruciale stap in de diagnose en behandeling van deze veel voorkomende kwaadaardige huidtumoren. Het stadiëren van mestceltumoren helpt dierenartsen de ernst van de ziekte te bepalen en de best mogelijke therapeutische maatregelen te plannen. Nauwkeurige stadiëring van mestceltumoren maakt het mogelijk onderscheid te maken tussen laaggradige en hooggradige tumoren, wat van groot belang is voor de prognose en de behandeling van de ziekte.
Het belang van het stadiëren van mestceltumoren
Mestceltumoren worden in stadium gebracht met behulp van een combinatie van klinische onderzoeken, histopathologische analyses en beeldvormingstechnieken. Deze uitgebreide stadiëring van mestceltumoren maakt het mogelijk om de verspreiding van de tumor in het lichaam te beoordelen en te bepalen of er uitzaaiingen aanwezig zijn.
Klinisch onderzoek en stadiëring van mestceltumoren
Een zorgvuldig klinisch onderzoek is de eerste stap bij het stadiëren van mestceltumoren. De dierenarts onderzoekt de knobbel op grootte, vorm, consistentie en locatie. Deze eerste observaties zijn belangrijk voor de verdere stadiëring van mestceltumoren.
Histopathologische analyse bij de stadiëring van mestceltumoren
De histopathologische analyse van het tumorweefsel is een centraal onderdeel van de stadiëring van mestceltumoren. Door biopsieën te onderzoeken kunnen de tumorcellen nauwkeurig worden gekarakteriseerd en in verschillende graden worden verdeeld. Deze cijfers zijn cruciaal voor de stadiëring van mestceltumoren en geven informatie over de agressiviteit van de tumor.
Beeldvormingsprocedures en stadiëring van mestceltumoren
Beeldvormingstechnieken zoals röntgenfoto's, echografie, CT en MRI spelen een belangrijke rol bij het stadiëren van mestceltumoren. Ze maken het mogelijk om de verspreiding van de tumor in het lichaam in beeld te brengen en de aanwezigheid van uitzaaiingen op te sporen. Deze informatie is essentieel voor een nauwkeurige stadiëring van mestceltumoren.
Fijne naaldaspiratie en de stadiëring van mestceltumoren
Fijne naaldaspiratie is een andere methode voor het stadiëren van mestceltumoren. Door cellen uit de tumor en regionale lymfeklieren te verzamelen en te onderzoeken, kan de stadiëring van mestceltumoren worden verfijnd.
Toepassing van stadiëring van mestceltumoren in therapie
De stadiëring van mestceltumoren heeft directe invloed op de therapiekeuze. Voor laaggradige tumoren, die als minder agressief worden geclassificeerd bij de stadiëring van mestceltumoren, kan chirurgische verwijdering vaak voldoende zijn. Voor hoogwaardige tumoren die bij de stadiëring van mestceltumoren als agressief en metastatisch worden geclassificeerd, zijn aanvullende behandelingen zoals bestralingstherapie en chemotherapie nodig.
Prognose gebaseerd op stadiëring van mestceltumoren
Stadiëring van mestceltumoren is ook cruciaal voor de prognose. Honden met laaggradige tumoren, die als minder gevaarlijk worden beschouwd bij de stadiëring van mestceltumoren, hebben doorgaans een goede prognose. Daarentegen hebben honden met hoogwaardige tumoren die als hoogwaardig zijn geclassificeerd bij de stadiëring van mestceltumoren een slechtere prognose vanwege de grotere kans op metastase en herhaling.
Conclusie
Stadiëring van mestceltumoren bij honden is een complex maar cruciaal proces voor de succesvolle diagnose en behandeling van deze tumoren. Door nauwkeurige stadiëring van mestceltumoren kunnen dierenartsen de juiste therapie kiezen en de prognose voor getroffen honden verbeteren. Door een uitgebreid klinisch onderzoek, histopathologische analyse, beeldvormingsprocedures en fijne naaldaspiratie kan de stadiëring van mestceltumoren worden geoptimaliseerd en kan de kwaliteit van leven en overlevingskansen van onze viervoeters aanzienlijk worden verbeterd.
Dergelijke onderwerpen komen uiteraard ook aan bod in onze chirurgiecursussen .
